Polare og ikke-polare dielektriske stoffer
I følge synspunktene til klassisk fysikk er dielektrikum fundamentalt forskjellig fra ledere, fordi det under normale forhold ikke er gratis elektriske ladninger i dem. Den totale ladningen til partiklene som danner dielektriske molekyler er null. Dette betyr imidlertid ikke i det hele tatt at molekylene til disse stoffene ikke er i stand til å utvise elektriske egenskaper.
Alle kjente lineære dielektrika kan deles inn i to store grupper: polare dielektriske og ikke-polare dielektriske stoffer. Denne inndelingen introduseres på grunn av forskjellene i polarisasjonsmekanismene til molekylene til hver type dielektrikum. Faktisk viser polarisasjonsmekanismen seg å være et ekstremt viktig aspekt i studiet av både de fysiske og kjemiske egenskapene til dielektrikum, og i studiet av deres elektriske egenskaper.
Ikke-polare dielektriske stoffer
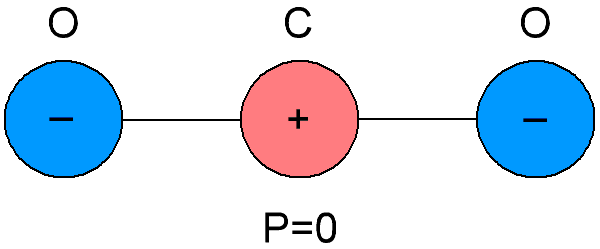
Ikke-polare dielektrika kalles også nøytrale dielektriske stoffer, fordi molekylene som disse dielektrikene er sammensatt av, er forskjellige i sammenfallet av tyngdepunktene til de negative og positive ladningene inne i dem.Som et resultat viser det seg at molekylene til ikke-polare dielektriske stoffer ikke har sitt eget elektriske moment, det er lik null. Og i fravær av et eksternt elektrisk felt, er de positive og negative ladningene til molekylene til slike stoffer ordnet symmetrisk.
Hvis et eksternt elektrisk felt påføres et ikke-polart dielektrikum, vil den positive og negative ladningen i molekylene forskyves fra deres opprinnelige likevektsposisjon, molekylene vil bli dipoler hvis elektriske momenter nå vil være proporsjonale med styrken til det elektriske felt brukt på dem, og vil bli rettet parallelt med feltet.
Eksempler på ikke-polare dielektriske stoffer som med hell brukes i dag som elektriske isolasjonsmaterialer er følgende: polyetylen, polystyren, hydrokarboner, petroleumsisolasjonsoljer, etc. Også lyse representanter for ikke-polare molekyler er for eksempel nitrogen, karbondioksid, metan, etc. MR.
Ikke-polare dielektriske stoffer, på grunn av deres lave tangensverdier for dielektriske tap, er mye brukt som høyfrekvente dielektriske i kondensatorer som K78-2.
Polar dielektrikk
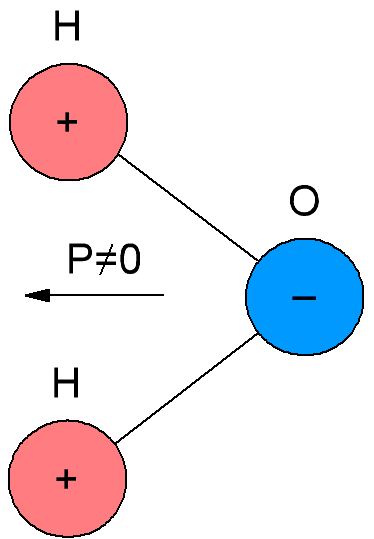
I polare dielektrika, som også kalles dipol-dielektriske, har molekylene sitt eget elektriske moment, det vil si at molekylene deres er polare. Årsaken er at molekylene til polare dielektriske stoffer har en asymmetrisk struktur, så massesentrene for negative og positive ladninger i molekylene til slike dielektrika faller ikke sammen.
Hvis i en ikke-polar polymer noen av hydrogenatomene erstattes av atomer av andre grunnstoffer eller av ikke-hydrokarbonradikaler, vil vi bare få et polart (dipol) dielektrisk, siden symmetrien vil bli brutt som et resultat av en slik erstatning. For å bestemme polariteten til et stoff ved dens kjemiske formel, må forskeren selvfølgelig ha en ide om den romlige strukturen til molekylene.
Når det ikke er noe eksternt elektrisk felt, er aksene til de molekylære dipolene orientert vilkårlig på grunn av termisk bevegelse, slik at på overflaten av dielektrikumet og i hvert element av dets volum er den elektriske ladningen i gjennomsnitt null. Men når et dielektrikum introduseres i et eksternt felt, oppstår en delvis orientering av molekylære dipoler.Som et resultat oppstår ukompenserte makroskopisk koblede ladninger på overflaten av dielektrikumet, og skaper et felt rettet mot det eksterne feltet.
Eksempler på polare dielektriske stoffer inkluderer følgende: klorerte hydrokarboner, epoksy- og fenolformaldehydharpikser, silisiumsilisiumforbindelser, etc. Vann- og alkoholmolekyler, for eksempel, er også bemerkelsesverdige eksempler på polare molekyler. Polar dielektrikum er mye brukt i forskjellige teknologifelt, som piezoelektrisk og ferroelektrisk, optikk, ikke-lineær optikk, elektronikk, akustikk, etc.

